醫學院胡小玉課題組發文揭示腸道上皮細胞轉錄延伸因子復合物NELF維持上皮屏障功能的新機制
點擊數:1671 時間:2021-11-03 16:32 來源:清華大學
清華新聞網10月28日電 上皮組織是哺乳動物隔離外界環境的第一道防線,而由腸道上皮細胞構成的腸道黏膜屏障可以幫助機體把腸腔環境中的病原體或共生微生物隔離開來。除了產生黏液層,這些腸上皮細胞構成一個連續的物理屏障,由緊密連接(tight junctions)、粘著連接(adherens junctions)以及橋粒(desmosomes)形成的上皮連接復合物構成。緊密連接的失調往往與腸道通透性增加和腸道炎癥相關,例如在炎癥性腸病(inflammatory bowel diseases, IBDs)患者中人們觀察到上皮細胞連接完整性出現異常,暗示細胞連接的異常可能參與了與IBDs的發病機制。細胞連接相關的基因表達需要被嚴格調控,以確保腸道上皮屏障的完整性。然而,控制腸道上皮細胞連接的轉錄調控機制至今未明。
以往對于腸道上皮細胞屏障功能的轉錄調控機制研究多集中在轉錄起始階段的序列特異性轉錄因子功能和表觀遺傳學修飾等,但是對于轉錄起始后(如轉錄延伸)調控是否參與腸道上皮細胞屏障功能的維持尚不清楚。轉錄起始后調控尤其是轉錄延伸負調控因子NELF復合物(negative elongation factor complex)參與的轉錄暫停過程,在多種生命過程中都起到重要作用。其中胡小玉課題組于2020年發文闡述了NELF在巨噬細胞活化過程中的動態變化及其調控巨噬細胞分泌細胞因子的關鍵作用(《自然·通訊》,2020)。這一研究結果暗示了NELF復合物可能在腸道上皮細胞穩態維持中也發揮了重要作用,于是,課題組研究人員通過構建Nelfb基因的腸道上皮細胞特異性缺陷小鼠,研究了NELF復合物介導的轉錄起始后調控機制在腸道上皮細胞中的功能。
10月25日,清華大學醫學院胡小玉課題組在《黏膜免疫》(Mucosal Immunology)期刊上在線發表了題為“上皮細胞轉錄延伸因子復合物通過維持腸道上皮細胞屏障功能完整性來改善結腸炎”(Epithelial NELF guards intestinal barrier function to ameliorate colitis by maintaining junctional integrity)的研究論文,揭示了轉錄延伸負調控因子NELF復合物通過調控細胞連接基因表達和抑制上皮細胞壞死來維持腸道上皮細胞屏障功能完整性,從而減緩結腸炎發病進程。
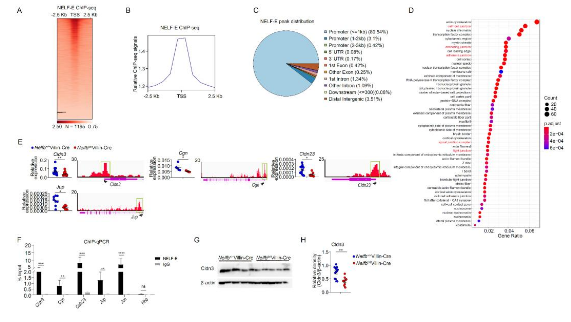
研究初期,課題組研究人員發現在穩態情況下,腸上皮NELF缺陷小鼠的腸上皮組織結構、細胞分化等未發生異常,但是在DSS構建的小鼠腸炎模型實驗中,NELF缺陷小鼠相較于對照組小鼠表現出顯著的體重下降和死亡率上升以及嚴重的組織損傷和免疫細胞浸潤等現象。隨后,研究人員嘗試探索NELF在緩解腸炎過程中發揮怎樣的作用,利用組織免疫熒光染色和透射電子顯微鏡等技術,發現DSS誘導腸炎早期(第二天)時,NELF缺陷小鼠的腸道上皮細胞便出現大量類似細胞壞死性(necroptosis)死亡。然而在抗生素處理之后,死亡細胞數量明顯減少,暗示NELF缺陷引起的上皮細胞死亡可能依賴于菌群刺激。進一步的細胞水平和分子水平上的探究發現,NELF缺陷小鼠在穩態條件下便出現部分上皮細胞死亡,并且是MLKL依賴的細胞壞死,而DSS作用加劇了上皮細胞的壞死。研究人員通過ChIP-seq等分子生物學手段發現,腸上皮NELF缺陷會導致大量上皮細胞特異性基因表達紊亂。值得注意的是,實驗結果顯示腸道上皮NELF可以通過直接靶向啟動子區域調控多種細胞連接相關基因(如Cldn3、Cgn、Cldn23、Jup等)的表達,并且在敲除NELF之后,細胞連接基因在mRNA和蛋白水平上顯著下調(圖1)。最后結合動物體內實驗和原位雜交(FISH)等技術驗證了在誘導性結腸炎早期階段,腸上皮NELF缺陷導致上皮通透性增加、共生菌入侵加劇,且腸炎發展依賴于共生菌入侵。
綜合上述實驗論證表明,在DSS誘導腸炎初期腸上皮NELF缺陷首先導致細胞連接相關基因顯著下調,促使上皮細胞屏障功能下降,加劇共生菌入侵以及共生菌依賴的上皮細胞壞死,而細胞壞死又進一步加劇了屏障破壞,最終引起嚴重的炎癥反應。該研究首次揭示了轉錄起始后階段轉錄延伸調控因子NELF復合物特異性調節腸道上皮屏障功能相關基因的表達,在維持腸道屏障穩態的過程中發揮了至關重要的作用。
清華大學醫學院教授胡小玉和醫學院助理研究員郭雪坤博士為本文的共同通訊作者,已畢業的博士生歐加堯和已出站的博士后管曉星博士為該論文共同第一作者。清華大學醫學院教授徐滬濟及其博士研究生王天嬌和胡小玉課題組的博士研究生王佳麗、張彬對本研究作出了重要貢獻。該研究得到了喬治·華盛頓大學教授李榮(Rong Li)的重要支持。該研究得到了國家自然科學基金委、科技部、清華大學-北京大學生命科學聯合中心以及清華大學免疫學研究所資助。